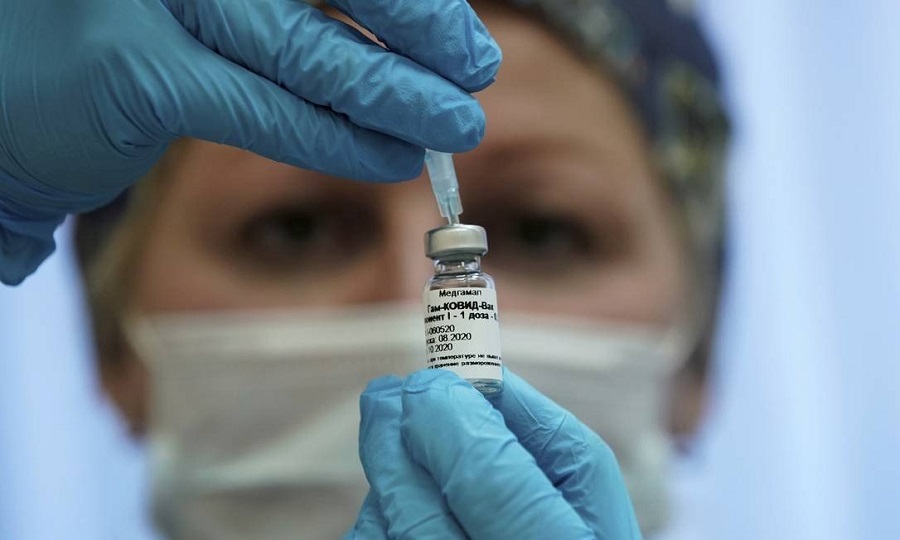
A Food and Drug Administration (FDA), equivalente à Anvisa nos EUA, liberou a AstraZeneca a retomar o braço norte-americano de seus testes da vacina da Universidade de Oxford contra o novo coronavírus. A informação é do Wall Street Journal (WSJ).
Segundo o jornal americano, a FDA concluiu o exame de dois casos de um possível efeito colateral neurológico em duas voluntárias. Um desses casos é o de uma britânica que teve mielite transversa, uma inflamação que ocorre na medula espinhal, descoberta em 8 de setembro. O outro não foi revelado.
A agência informou à AstraZeneca na sexta-feira que o último estágio do teste nos EUA pode ser retomado. O FDA, ainda segundo o WSJ, não conseguiu descobrir se a vacina foi a causa das reações nas duas pacientes, embora também não pudesse descartar uma ligação, disse a fonte do jornal.
“A agência planeja exigir que os pesquisadores informem os voluntários sobre os casos e os monitorem para quaisquer eventos neurológicos relacionados, como dormência (por exemplo)”, diz a reportagem, que ouviu fontes ligadas à investigação e teve acesso a documentos da FDA.
Depois disso, os testes foram retomados em 12 de setembro no Reino Unido e em 14 de setembro no Brasil. No entanto, a Food and Drug Administration (FDA) conduziu uma investigação independente, concluída finalmente nesta semana.
Nesta quarta-feira, o médico brasileiro João Pedro Feitosa, que participava do teste da vacina, morreu de Covid-19, mas a Universidade de Oxford determinou que não havia “nenhuma preocupação de segurança” com a vacina. A Anvisa também não viu razão para interromper os estudos. Segundo fontes ligadas ao estudo, ele havia tomado o placebo.
Liberação no Brasil
Em setembro, um comitê independente brtânico avaliou a situação da paciente inglesa e concluiu que não havia relação causal entre a vacina e a mielite transversa diagnosticada em uma das 18 mil pessoas que participaram do estudo.
No Brasil, o estudo envolve cinco mil voluntários. Os ensaios são coordenados pela Universidade Federal de São Paulo (Unifesp), por meio do Centro de Referência para Imunobiológicos Especiais (Crie/Unifesp).
No Rio e em Salvador, os estudos são realizados e financiados pelo Instituto D’Or.
Os técnicos da Anvisa avaliaram uma série de informações recebidas da agência reguladora britânica (MHRA), do Comitê Independente de Segurança do Estudo Clínico e da AstraZeneca. Foram analisados vários fatores, como a causalidade e o conjunto de dados de segurança gerados no estudo. [Capa: Tatyana Makeyeva/File Photo/Reuters]