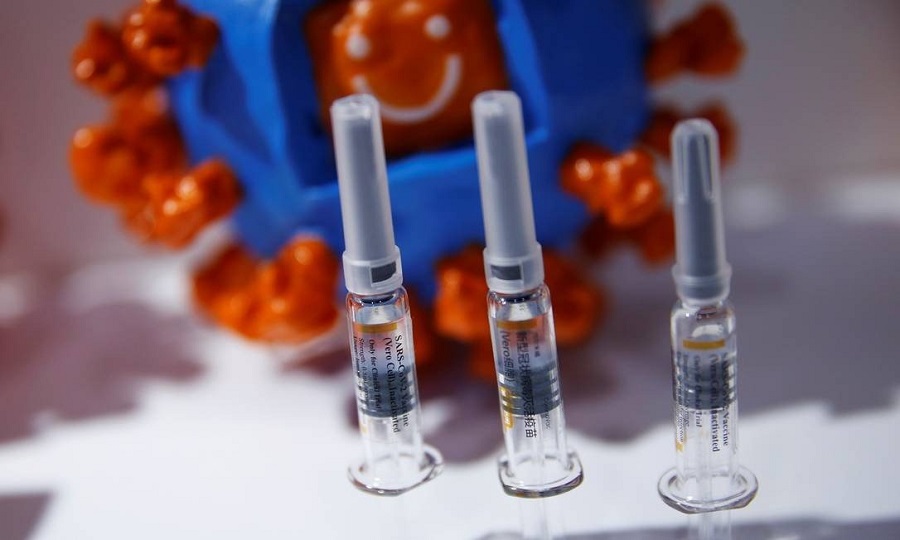
O Comitê Internacional Independente, que analisa os estudos da vacina CoronaVac, desenvolvida pela empresa chinesa Sinovac em parceria com o Instituto Butantan, emitiu parecer pela retomada dos testes no Brasil. A documentação chegou à Agência Nacional de Vigilância Sanitária (Anvisa) nesta terça-feira (10), por volta das 17h.
Na última segunda, a Anvisa determinou a paralisação dos testes, o que abriu um embate com o Instituto Butantan, que considerou a decisão desacertada. A ausência de nexo causal entre o evento adverso grave com um voluntário e a vacina é um dos fatores apontados.
A Anvisa assinalou, em entrevista coletiva nesta terça-feira, que o parecer deveria ter sido enviado junto com a comunicação, feita pelo Butantan na última sexta-feira, do evento adverso grave. Os órgãos não dão detalhes sobre o episódio por questão de confidencialidade. O evento adverso, no entanto, foi a morte de um participante por suicídio.
O parecer traz dados e datas que agora serão analisados pela Anvisa. Um grupo de técnicos começou a avaliar o documento em inglês. Mas a expectativa é de que a decisão não saia ainda nesta terça-feira.
Horas antes de receber o documento, o diretor-presidente da Anvisa, Antonio Barra Torres, disse que o estudo continuaria suspenso até que a agência tivesse todas as informações sobre a morte do voluntário. Ele afirmou que as informações do Butantan eram “insuficientes e incompletas” e que, por isso, a agência decidiu pela suspensão dos estudos.
— As informações veiculadas ontem [segunda-feira] foram consideradas, pela área técnica, insuficientes, incompletas, para que ontem fosse possível, de posse delas, continuar permitindo o desenvolvimento vacinal — disse Barra.
A diretora da Anvisa responsável pela área de vacinas, Alessandra Bastos, reforçou que a decisão foi técnica e seguiu protocolos internacionais.
— Gostaria que isso ficasse muito claro: diante de um efeito adverso grave não esperado, suspende o estudo clínico. Diante de um efeito adverso grave esperado, segue com o estudo — explicou a diretora Alessandra Bastos.
O diretor do Instituto Butantan, Dimas Covas, reagiu nesta terça-feira, dizendo em coletiva de imprensa que a decisão da Anvisa causou indignação. Segundo ele, o evento não tem relação com os testes da CoronaVac.
– Do ponto de vista clínico do caso, é impossível que haja relacionamento do evento com a vacina. Essa definição (impossível) encerra a discussão – salientou o presidente do Butantan.
O diretor disse ainda que a decisão da agência causou “incerteza” e “medo” nas pessoas.
– Causaram incerteza, medo nas pessoas, fomentaram um ambiente que já não estava propício devido ao fato dessa vacina ser feita em associação com a China – declarou o diretor do instituto.
O documento do Comitê Internacional foi recebido pelo Conselho Nacional de Ética em Pesquisa (Conep), ligado ao Ministério da Saúde, que também acompanha o desenvolvimento dos estudos. Diferentemente da Anvisa, ao ser notificado na sexta-feira passada pelo Butantan, a Conep não recomendou a suspensão dos estudos. E manterá essa posição, após receber o documento do comitê.
— Vamos fazer um parecer com calma, mas claro na direção que o evento não justifica a suspensão. A retomada do estudo depende unicamente da Anvisa — disse Jorge Venâncio ao GLOBO.
Pesquisas como as de vacinas precisam passar pelo aval da Anvisa e da Conep, tanto no momento de serem autorizadas quanto na retomada após a suspensão dos testes. A Anvisa faz uma análise mais voltada para a questão sanitária, de eficácia e segurança. A Conep atua também na segurança e na defesa dos direitos de quem participa dos experimentos. Se um dos órgãos veta um teste, ele não pode ser feito.
Mais cedo, antes de receber o parecer do Comitê Internacional Independente, o coordenador da comissão, Jorge Venâncio, disse que o órgão avaliou os dados preliminares reportados pelo Instituto Butantan em relação à morte do voluntário e entendeu que os estudos não deveriam ter sido suspensos. Segundo ele, o falecimento do voluntário não teria relação com a aplicação da vacina.
— Não pedimos suspensão de estudo, de jeito nenhum. O voluntário tomou a segunda dose da vacina 22 dias antes, não tinha nenhum problema de saúde e chegou a fazer um check-up particular, com uma batelada de exames, pouco depois. Então não tem nenhuma lógica suspender um estudo que mobiliza milhares de pessoas para uma vacina que precisamos desesperadamente — disse Venâncio. [Capa: Tingshu Wang/Reuters]