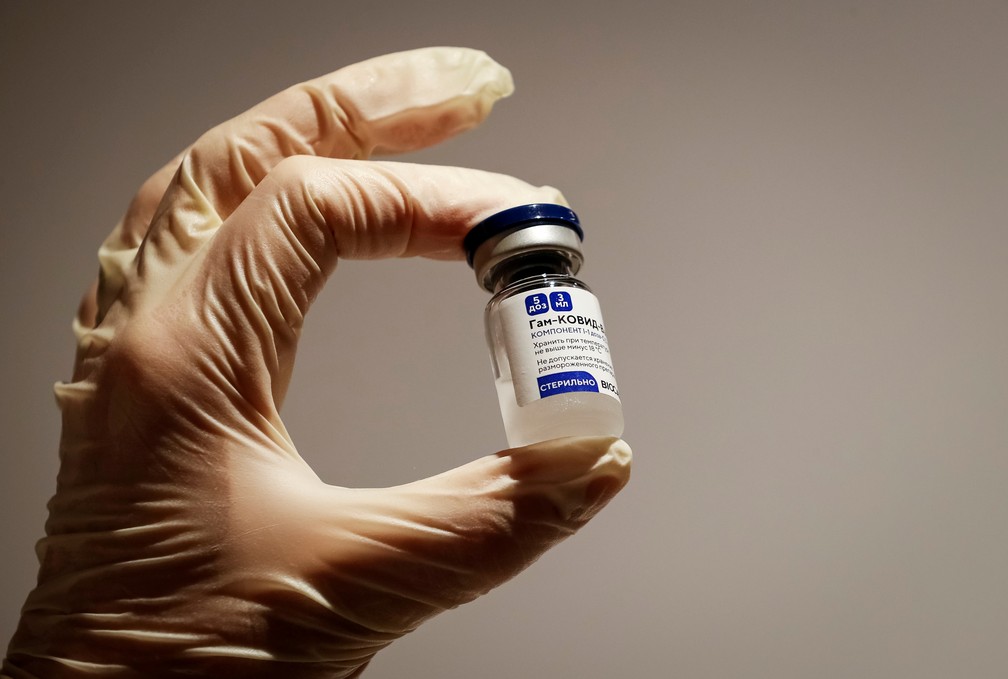
A Agência Nacional de Vigilância Sanitária (Anvisa) recebeu nesta sexta-feira (26) um novo pedido de uso emergencial para a vacina Sputnik V.
A Anvisa informou em um comunicado que o pedido anterior feito pelo laboratório União Química –que representa, no Brasil, o Fundo Russo desenvolvedor do imunizante – será cancelado.
No início desta semana, a agência reguladora disse que precisava ter acesso aos dados brutos dos testes da vacina, um requisito para o pedido de uso emergencial no país.
Segundo a agência, os documentos para este novo pedido foram entregues à Anvisa durante a madrugada e sua equipe faz a triagem do pedido.
A Anvisa tem até sete dias para a conclusão da análise caso os técnicos da organização não apresentem nenhum questionamento em relação ao material apresentado.
“A análise do pedido de uso emergencial é feita por uma equipe multidisciplinar, envolve especialistas das áreas de registro, monitoramento e inspeção”, disse a agência em nota.
Até o momento, o país tem usado apenas duas vacinas contra Covid-19, a CoronaVac, produzida em parceria com o Instituto Butantan, e a AstraZeneca/Oxford.
A vacina da Pfizer já obteve registro definitivo pela Anvisa e foi comprada pelo governo, mas a entrega do primeiro lote ocorrerá apenas em abril.
Sputnik V
A vacina russa Sputnik V, desenvolvida pelo Instituto Gamaleya, foi autorizada para uso emergencial pelo governo russo antes mesmo do fim dos estudos clínicos.
A vacina já foi aprovada para uso na Argentina e em outros países da América Latina.
O Ministério da Saúde anunciou um acordo para comprar 10 milhões de doses desta vacina para integrar o Plano Nacional de Imunização.
Além disso, governadores do Consórcio do Nordeste anunciaram a assinatura de compra de mais 37 milhões de doses da vacina russa.